Skrócenia okresu ważności pozwoleń
Niektóre produkty lecznicze są skreślane z Rejestru na wniosek podmiotów odpowiedzialnych. Wykaz produktów leczniczych usuniętych z centralnego unijnego rejestru prowadzi i publikuje na bieżąco Komisja Europejska. Natomiast Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych od roku 2012 przygotowuje miesięczne (lub czasami zbiorcze kilkumiesięczne) zestawienia produktów leczniczych skreślonych z rejestru na wniosek podmiotów odpowiedzialnych, jednak nie publikuje ich na swojej stronie internetowej lub w Biuletynie Informacji Publicznej, lecz jedynie udostępnia Ministerstwu Zdrowia, Głównemu Inspektoratowi Farmaceutycznemu, Narodowemu Funduszowi Zdrowia i Naczelnej Izbie Aptekarskiej.
W roku 2021 Prezes Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych wydał, na wniosek podmiotów odpowiedzialnych, 486 decyzji o skróceniu okresu ważności pozwolenia (2020: 437; 2019: 569; 2018: 418; 2017: 360; 2016: 337; 2015: 432; 2014: 506; 2013: 862; 2012: 545), oznaczających skreślenie z Rejestru 235 marek produktów leczniczych (2020: 228; 2019: 256; 2018: 207; 2017: 159; 2016: 161; 2015: 168; 2014: 197; 2013: 308; 2012: 254). Liczby te stanowią odpowiednio 75% i 61% w stosunku do wydanych w roku 2021 decyzji rejestracyjnych i zarejestrowanych marek produktów leczniczych (2020: 93% i 81%; 2019: 88% i 75%; 2018: 71% i 64%; 2017: 44% i 35%; 2016: 46% i 39%; 2015: 64% i 43%; 2014: 84% i 59%; 2013: 110% i 73%; 2012: 43% i 41%).
W roku 2021 Komisja Europejska wycofała z unijnego Rejestru, na wniosek podmiotów odpowiedzialnych, 26 marek produktów leczniczych (2020: 20; 2019: 24; 2018: 24; 2017: 13; 2016: 12; 2015: 11; 2014: 14; 2013: 10; 2012: 19), co stanowi 29% w stosunku do liczby zarejestrowanych marek produktów leczniczych (2020: 22%; 2019: 38%; 2018: 26%; 2017: 14%; 2016: 15%; 2015: 12%; 2014: 14%; 2013: 12%; 2012: 29%).
Powyższe liczby nie obejmują produktów leczniczych, dla których ważność pozwoleń wygasa z mocy prawa na skutek nie złożenia przez podmiot odpowiedzialny wniosku o rerejestrację lub na skutek nie wprowadzenia na rynek w ciągu 3 lat od rejestracji (sunset clause).
Tabela 22. Liczba wydanych decyzji o skróceniu okresu ważności pozwolenia produktów leczniczych w poszczególnych miesiącach roku 2021.
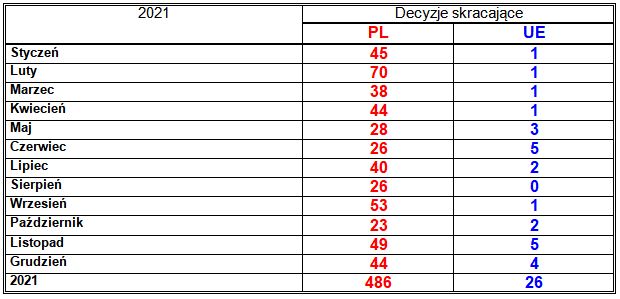
Tabela 23. Podział marek produktów leczniczych, dla których w 2021 roku skrócono okres ważności pozwolenia, według pierwszego poziomu klasyfikacji ATC (14 klas).
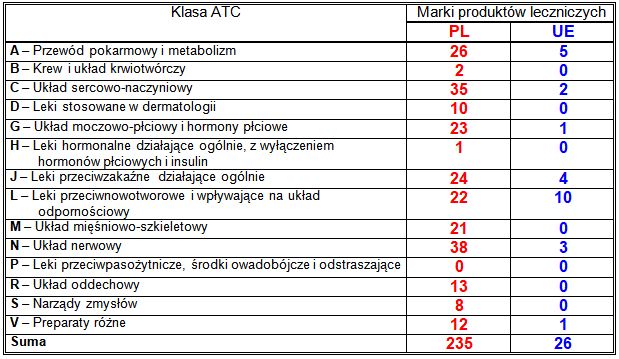
Tabela 24. Podział marek produktów leczniczych, dla których w 2021 roku skrócono okres ważności pozwolenia, według kategorii dostępności.
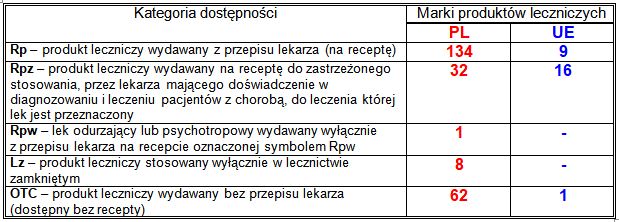
Kategorie dostępności Rpw i Lz występują tylko w polskim systemie prawnym – ich odpowiednikiem w przepisach europejskich jest kategoria dostępności Rpz.
Tabela 25. Podmioty odpowiedzialne, na wniosek których skrócono w Polsce w 2021 roku okres ważności pozwoleń dla największej liczby marek produktów leczniczych.
| Podmiot odpowiedzialny | Marki produktów leczniczych |
| Mylan | 23 |
| Heel | 18 |
| Accord Healthcare | 16 |
| Stada | 15 |
| Sandoz | 13 |
| Alvogen | 11 |
| GlaxoSmithKline | 10 |
| Teva | 8 |
Tabela 26. Podmioty odpowiedzialne, na wniosek których wycofano z unijnego Rejestru w 2021 roku najwięcej marek produktów leczniczych.
| Podmiot odpowiedzialny | Marki produktów leczniczych |
| Teva | 5 |
| Merck Sharp & Dohme | 4 |
| Mylan | 2 |
| Takeda | 2 |
Skrócenia okresu ważności pozwoleń wynikają najczęściej ze zmian polityki marketingowej firm farmaceutycznych, a także zmniejszenia zapotrzebowania na niektóre starsze leki zastępowane przez leki nowsze i lepsze lub zmniejszenia poziomu sprzedaży i opłacalności produkcji przy dużej konkurencji leków, rejestrowanych często w dużej liczbie marek dla tej samej substancji czynnej. Ponadto na skutek łączenia się firm farmaceutycznych następuje korekta asortymentu leków w połączonej firmie, skutkująca najczęściej skreśleniem z Rejestru jednej z dublujących się marek leków o tej samej substancji czynnej.
Liczba skreślonych z Rejestru marek leków w ramach klas terapeutycznych i substancji czynnych jest także pochodną liczby marek dotychczas zarejestrowanych. Najwięcej skróceń okresu ważności pozwoleń dotyczyło następujących grup produktów:
- w Rejestrze polskim:
- klasa A – przeciwcukrzycowy glimepiryd (3 marki), inhibitory pompy protonowej (3 marki), w tym omeprazol (2 marki);
- klasa B – każde ze skróconych pozwoleń zawierało inne substancje czynne;
- klasa C – inhibitory konwertazy angiotensyny (5 marek), w tym peryndopryl (2 marki) i ramipryl (2 marki); inhibitory reduktazy hydroksymetyloglutarylo-koenzymu A (5 marek), w tym atorwastatyna (2 marki); blokery receptora angiotensyny II (4 marki), w tym losartan (2 marki) i walsartan (2 marki); blokery receptora angiotensyny II w połączeniach z lekami moczopędnymi (3 marki), w tym walsartan z hydrochlorotiazydem (2 marki); inhibitory konwertazy angiotensyny w połączeniach z blokerami kanału wapniowego (3 marki), w tym enalapryl z lerkanidypiną (2 marki); moczopędny indapamid (2 marki); wpływające na stężenie lipidów ezetymib (2 marki) oraz połączenie rosuwastatyny z ezetymibem (2 marki);
- klasa D – każde ze skróconych pozwoleń zawierało inne substancje czynne;
- klasa G – urologiczne leki przeciwskurczowe (6 marek), w tym solifenacyna (4 marki) i tolterodyna (2 marki); dopochwowe środki antykoncepcyjne zawierające połączenie etonorgestrelu z etinylestradiolem (2 marki); stosowane w łagodnym przeroście gruczołu krokowego połączenie tamsulozyny z dutasterydem (2 marki);
- klasa H – antagonista hormonów przytarczyc kalcytonina (1 marka);
- klasa J – przeciwwirusowe nukleozydowe i nukleotydowe inhibitory odwrotnej transkryptazy (6 marek), w tym entekawir (5 marek); stosowane w leczeniu zakażeń wirusem HIV połączenie lamiwudyny z abakawirem (3 marki); przeciwwirusowe połączenia dizoproksylu tenofowiru z emtrycytabiną (2 marki) oraz emtrycytabiny z dizoproksylem tenofowiru i efawirenzem (2 marki); przeciwbakteryjny linezolid (2 marki); przeciwgrzybiczy lipopeptyd kaspofungina (2 marki);
- klasa L – inhibitory kinazy tyrozynowej receptora naskórkowego czynnika wzrostu (6 marek), w tym erlotynib (5 marek); inhibitor kinazy ssaków ewerolimus (2 marki); przeciwnowotworowy anagrelid (2 marki);
- klasa M – niesteroidowe leki przeciwzapalne i przeciwreumatyczne (9 marek), w tym meloksykam (3 marki) i ibuprofen (2 marki); bifosfoniany wpływające na strukturę i mineralizację kości (4 marki), w tym kwas ibandronowy (2 marki);
- klasa N – leki przeciwpadaczkowe (5 marek), w tym lakosamid (2 marki); połączenie opioidu tramadolu z przeciwbólowym i przeciwgorączkowym paracetamolem (3 marki); paracetamol w połączeniach (4 marki), w tym z pseudoefedryną (2 marki); przeciwmigrenowy selektywny agonista serotoniny ryzatryptan (3 marki); neuroleptyk arypiprazol (2 marki);
- klasa R – przeciwkaszlowe dekstrometorfan (2 marki) i butamirat (2 marki);
- klasa S – każde ze skróconych pozwoleń zawierało inne substancje czynne;
- klasa V – leki homeopatyczne (11 marek);
- w Rejestrze unijnym:
- klasa A – przeciwcukrzycowa pochodna tiazolidynedionu pioglitazon (3 marki);
- klasa J – lek przeciwwirusowy stosowany w leczeniu zakażeń HIV rybawiryna (2 marki);
- klasa L – przeciwnowotworowe przeciwciała monoklonalne (4 marki), w tym bewacyzumab (2 marki); pobudzające układ odpornościowy interferony (3 marki), w tym peginterferon alfa-2b (2 marki);
- w pozostałych klasach – każde ze skróconych pozwoleń zawierało inne substancje czynne.
Opracowanie: dr n. farm. Jarosław Filipek
Kierownik Działu Informacji o Produktach
Administrator Farmaceutycznej Bazy Danych BAZYL
Przygotowanie zestawienia szczegółowego: Krystyna Skrzyńska
IQVIA
2022-04-15
Źródła:
– nomenklatura nazw substancji czynnych oraz klasyfikacja ATC na podstawie opracowania WHO Collaborating Centre for Drug Statistics Methodology (“Guidelines for ATC Classification and DDD assignment 2021”, Oslo 2020; “ATC Index with DDDs 2021”, Oslo 2020), ze zmianami i uzupełnieniami mającymi zastosowanie w roku 2021 – tłumaczenie własne;
– nomenklatura nazw substancji czynnych dla preparatów roślinnych, galenowych i szczepionek: „Farmakopea Polska XII”; “Urzędowy Wykaz Produktów Leczniczych Dopuszczonych do Obrotu na Terytorium Rzeczypospolitej Polskiej”;
– informacje rejestracyjne PL: “Urzędowy Wykaz Produktów Leczniczych Dopuszczonych do Obrotu na Terytorium Rzeczypospolitej Polskiej”; miesięczne wykazy zarejestrowanych produktów leczniczych publikowane w Biuletynie Informacji Publicznej Urzędu Rejestracji PLWMiPB; pozwolenia i decyzje porejestracyjne nadsyłane przez podmioty odpowiedzialne; wykazy produktów leczniczych, którym skrócono okres ważności pozwolenia;
– informacje rejestracyjne UE: “Community register of medicinal products for human use”; “Community list of not active medicinal products for human use”;
– informacje o wprowadzeniu produktu na rynek w Polsce: dane IQVIA;
– pozostałe opinie i komentarze: autorskie.










