Podsumowanie
Reasumując, chlorheksydyna wykazuje doskonałą aktywność wobec bakterii i grzybów, jako antyseptyk stosowany do odkażania skóry i błon śluzowych w tym rąk, jednak jej aktywność wobec niektórych wirusów jest ograniczona (Tabela 4). Dlatego wskazane jest jej stosowanie łączne z etanolem, aby rozszerzyć spektrum działania o tę grupę patogenów. Roztwory etanolowe chlorheksydyny funkcjonujące w recepturze jako leki magistralne, spełniają więc najwyższe standardy, jeśli chodzi o zabezpieczenie antyseptyczne, również w stosunku do wszystkich wirusów istotnych klinicznie (albowiem są to roztwory 96% etanolu). Jednocześnie warto podkreślić, że chlorheksydyna wykazuje wysoki profil bezpieczeństwa i jest na ogół dobrze tolerowana.
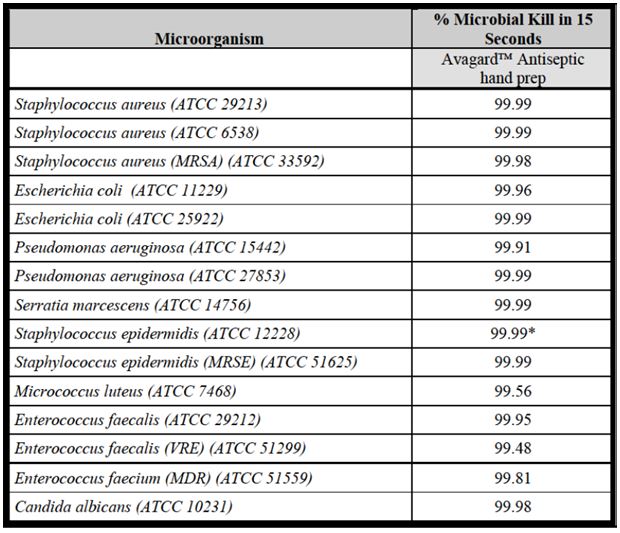
Tabela 1: Aktywność antybakteryjna 1% roztworu glukonianu chlorheksydyny w etanolu 68,7 % (v/v) (2)
| Drobnonustroje | Średnia redukcja log 0.05% chlorheksydyna po 20 sekundach | Średnia redukcja log 0.05% chlorheksydyna po 60 sekundach | Średnia redukcja log 0.05% chlorheksydyna po 600 sekundach |
| Gram (+) ziarenkowce | |||
| Staphylococcus aureus | 0.4 | 0.7 | 2.5 |
| Staphylococcus epidermidis | 2.2 | 3.4 | >5.1 |
| Streptococcus faecalis | 0.4 | 0.4 | 1.1 |
| Streptococcus pneumoniae | 0.8 | 1.5 | >3.5 |
| Streptococcus pyogenes | 1.2 | 1.8 | >3.7 |
| Streptococcus viridans | 0.4 | 0.8 | 2.3 |
| Gram (+) pałeczki | |||
| Bacillus subtilis | 0.5 | 0.5 | 0.3 |
| Clostridium welchii | 2.1 | 3.1 | >4.8 |
| Corynebacterium spp | 1.1 | 1.4 | 3.7 |
| Lactobacillus casei | 0.2 | 0.2 | 4.1 |
| Listeria monocytogenes | 0.6 | 2.2 | 4.8 |
| Gram (-) | |||
| Acinetobacter anitratus | 1.4 | 2.6 | >5.3 |
| Bacteroides distastonis | 0.9 | 2.7 | >4.9 |
| Bacteroides fragilis | 3.0 | 4.2 | 5.2 |
| Campylobacter pyloridis | 2.8 | >4.0 | |
| Escherichia coli | 3.2 | 5.0 | >6.4 |
| Haemophilus influenzae | >4.1 | >4.1 | >4.1 |
| Klebsiella aerogenes | 2.7 | 3.9 | >5.9 |
| Klebsiella pneumoniae | 3.0 | 4.8 | >6.2 |
| Proteus mirabilis | 0.8 | 0.9 | 2.9 |
| Proteus vulgaris | 0.8 | 1.0 | 4.1 |
| Pseudomonas aeruginosa | 1.7 | 2.7 | 4.9 |
| Salmonella typhimurium | 2.0 | 3.7 | >6.0 |
| Grzyby/ pleśnie | |||
| Aspergillus fumigatus | 0.7 | 1.2 | 2.4 |
| Aspergillus niger | 0.7 | 1.2 | 3.0 |
| Penicillium notatum | 0.6 | 2.0 | 3.5 |
| Rhizopus sp | 0.4 | 0.4 | 0.5 |
| Scopulariopsis spp | 0.6 | 1.1 | 2.3 |
| Drożdżaki | |||
| Candida albicans | 2.8 | >4.1 | >4.2 |
| Candida guillermondii | 3.5 | >4.3 | >4.3 |
| Candida parapsilosis | 2.1 | 3.4 | >4.2 |
| Candida pseudotropicalis | 3.6 | >4.4 | >4.4 |
| Cryptococcus neoformans | 4.0 | >4.2 | >4.2 |
| Prototheca zopfii | 3.3 | >3.6 | >3.6 |
| Saccharomyces cerevissia | 3.7 | >3.7 | >3.7 |
| Torulopsis glabrata | 1.3 | 2.2 | >4.4 |
| Dermatofity | |||
| Epidermophyton floccosum | 0.7 | 0.5 | >1.8 |
| Microsporum canis | 0.4 | 1.0 | >2.0 |
| Microsporum fulvum | 0.2 | 0.6 | >2.4 |
| Microsporum gypseum | 0.1 | 0.3 | 2.0 |
| Trichophyton equinum | 0.5 | 1.1 | >2.1 |
| Trichophyton interdigitale | 0.4 | 0.9 | >2.4 |
| Trichophyton mentagrophytes | 1.3 | >2.1 | >2.1 |
| Trichophyton quinkeanum | 0.2 | 0.9 | >2.8 |
| Trichophyton rubrum | 0.3 | 0.6 | >2.4 |
| Trichophyton tonsurans | 0.4 | 0.3 | 1.6 |
| Wirus | Rodzina | Aktywność | Chlorheksydyna (%) |
| Respiratory syncytia virus (RSV) | Paramyxovirus | + | 0.25 |
| Herpes hominis/simplex (HSV) | Herpesvirus | + | 0.25 |
| Polio virus type 2 (PV2) | Enterovirus | – | 0.02 |
| Adenovirus type 2 | Adenovirus | – | 0.02 |
| Equine infectious anaemia virus (EIAV) | Retrovirus | + | 2.0 |
| Variola virus (wirus ospy prawdziwej) (VARV) | Poxvirus | + | 2.0 |
| Herpes simplex virus type 1/type 2 (HSV-1, HSV-2) | Herpesvirus | + | 0.02 |
| Wirus końskiej grypy | Orthomyxovirus | + | 0.001 |
| Wirus klasycznego pomoru świń (ASF) | Togavirus | + | 0.001 |
| Wirusowa biegunka bydła (BVD) | Paramyxovirus | + | 0.001 |
| Wirus paragrypy | Paramyxovirus | + | 0.001 |
| Wirus epidemicznej biegunki (TEGV) | Coronavirus | + | 0.001 |
| Wirus wścieklizny | Rhabdovirus | + | 0.001 |
| Nosówka (CDV) | Paramyxovirus | + | 0.01 |
| Wirus ptasiego zapalenia oskrzeli (IBV) | Coronavirus | + | 0.01 |
| Newcastle virus (VND) | Paramyxovirus | + | 0.01 |
| Choroba Aujeszkiego | Herpesvirus | + | 0.01 |
| Cytomegalovirus (CMV) | Herpesvirus | + | 0.1 |
| Coxsackie virus | Picornavirus | – | 0.4 |
| Echo virus | Picornavirus | – | 0.4 |
| Rotawirus | Reovirus | – | 1.5 |
| Ludzki wirus niedoboru odporności (HIV) | Retrovirus | + | 0.2 |
Artykuł przygotowany we współpracy z firmą Fagron

Piśmiennictwo:
- Karpinski TM, Szkaradkiewicz AK (2015) Chlorhexidine–pharmaco-biological activity and application. Eur Rev Med Pharmacol Sci. 19(7):1321-6.
- FDA Approved Drug Products: Avagard (chlorhexidine/ethyl alcohol) topical solution [Link]
- Mohammadi Z, Abbott PV (2009) The properties and applications of chlorhexidine in endodontics. Int Endod J. 42(4):288-302. doi: 10.1111/j.1365-2591.2008.01540.x. [PubMed:19220510].
- Gomes BPFA, Souza SFC, Ferraz CCR et al. (2003) Effectiveness of 2% chlorhexidine gel and calcium hydroxide against Enterococcus faecalis in bovine root dentine in vitro. Int Endod J 36:267–75.
- FDA Approved Drug Products: Peridex (chlorhexidine gluconate) oral rinse [Link]
- National Committee for Clinical Laboratory Standards, “Methods for Dilution Antimicrobial Susceptibility Test for Bacteria that Grow Aerobically”, Document M7-A2, Vol. 5 (22).
- Charles D, Heal CF, Delpachitra M, Wohlfahrt M, Kimber D et al. (2017) Alcoholic versus aqueous chlorhexidine for skin antisepsis: the AVALANCHE trial. CMAJ 189(31): E1008–16. doi:10.1503/cmaj.161460.
- Darouiche RO, Wall MJ Jr, Itani KM, Otterson MF, Webb AL et al. (2010) Chlorhexidine-Alcohol versus Povidone-Iodine for Surgical-Site Antisepsis. N Engl J Med 362(1):18-26. doi: 10.1056/NEJMoa0810988.
- Chiewchalermsri C, Sompornrattanaphan M, Wongsa C, Thongngarm T. (2020) Chlorhexidine Allergy: Current Challenges and Future Prospects. J Asthma Allergy 13:127-33. doi: 10.2147/JAA.S207980.
- Springel EH, Wang XY, Sarfoh VM, Stetzer BP, Weight SA, Mercer BM (2017) A randomized open-label controlled trial of chlorhexidine-alcohol vs povidone-iodine for caesarean antisepsis: the CAPICA trial. Am J Obstet Gynecol. 217(4):463. e1-463.e8. doi: 10.1016/j.ajog.2017.05.060.
- Noorani A, Rabey N, Walsh SR, Davies RJ (2010). Systematic review and meta-analysis of preoperative antisepsis with chlorhexidine versus povidone-iodine in clean-contaminated surgery. Br J Surg 97(11):1614–20. doi:10.1002/bjs.7214.
- Dumville JC, McFarlane E, Edwards P, Lipp A, Holmes A, Liu Z (2015) Preoperative skin antiseptics for preventing surgical wound infections after clean surgery. Cochrane Database Syst Rev (4):CD003949. doi: 10.1002/14651858.CD003949.pub4.
- Chen S, Chen JW, Guo B, Xu CC (2020) Preoperative Antisepsis with Chlorhexidine Versus Povidone-Iodine for the Prevention of Surgical Site Infection: a Systematic Review and Meta-analysis. World J Surg 44(5):1412-24. doi: 10.1007/s00268-020-05384-7.
- Farmakopea Polska XI. Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, Warszawa 2017.
- Rose MA, Garcez T, Savic S, Garvey LH (2019) Chlorhexidine allergy in the perioperative setting: a narrative review. Br J Anaesth 123(1):e95–e103. doi:10.1016/j.bja.2019.01.033 [PubMed].
- Opstrup MS, Johansen JD, Zachariae C, Garvey LH (2016) Contact allergy to chlorhexidine in a tertiary dermatology clinic in Denmark. Contact Dermatitis 74(1):29–36. doi:10.1111/cod.2016.74.issue-1 [PubMed]
- https://www.drugs.com/sfx/chlorhexidine-topical-side-effects.html.
- Chiang SR, Jung F, Tang HJ, Chen CH, Chen CC, Chou HY, Chuang YC (2018) Desiccation and ethanol resistances of multidrug resistant Acinetobacter baumannii embedded in biofilm: The favorable antiseptic efficacy of combination chlorhexidine gluconate and ethanol. J Microbiol Immunol Infect 51(6):770-7.
- Bhardwaj P, Ziegler E, Palmer KL (2016) Chlorhexidine Induces VanA-Type Vancomycin Resistance Genes in Enterococci Antimicrob Agents Chemother 60(4): 2209–21. doi:10.1128/AAC.02595-15.
- Eggers M, Koburger-Janssen T, Ward LS, Newby C, Müller S (2018) Bactericidal and Virucidal Activity of Povidone-Iodine and Chlorhexidine Gluconate Cleansers in an In Vivo Hand Hygiene Clinical Simulation Study. Infect Dis Ther 7(2):235-247. doi: 10.1007/s40121-018-0202-5.
- Kampf G (2018) Efficacy of ethanol against viruses in hand disinfection. J Hosp Infect 98:331–338. doi: 10.1016/j.jhin.2017.08.025. [PMC free article].
- Lim KS, Kam PC (2008) Chlorhexidine–pharmacology and clinical applications. Anaesth Intensive Care 36(4):502-12.











